By Marko Originally Posted Monday, September 10, 2007
MALARIA
Marko caoos@hotmail.com

Il nome “malaria” è legato alla credenza degli antichi romani che questa malattia fosse causata dall’aria cattiva delle paludi che circondavano Roma.
Secondo una leggenda vietnamita, le zanzare nacquero dalla triste storia amorosa di un amante tradito; in un villaggio sulle palafitte, una sposa si ammalò e mori in pochi giorni. Il genio della palude, commosso dal pianto dello sposo, punse il suo dito, e da una goccia di sangue trasse la vita per la fanciulla morta. La sposa tornò in vita ed i due sposi vissero un periodo di felicità…Una sera la sposa fuggì tradendolo, insensibile alle preghiere del marito, si punse il dito restituendogli quella goccia di sangue. Improvvisamente il suo corpo divenne polvere, questa cadde nell’acqua della palude e si animò; cosi nacquero le larve di zanzara. Ancora oggi la sposa non si rassegna al suo destino, ogni notte punge, con la speranza che la goccia di sangue posso restituirle la vita……
Oggi sappiamo che la malaria è una malattia parassitaria causata dal plasmodio trasmesso dalla puntura della zanzara anopheles femmina infetta.
La malaria è un problema che coinvolge oltre 100 paesi nel mondo, nei quali abitano circa 3 miliardi di persone e che rappresentano circa il 50% della popolazione mondiale, soprattutto bambini sotto i 5 anni e donne incinte. La malaria uccide un bambino ogni 30 secondi.
Le ultime stime dicono che annualmente ci sono 1,5 milioni di morti e 300-500 milioni di casi.
E’ stata stimata la perdita economica annuale, nei paesi dove è endemica la malaria, in circa l’1,3 % del pil.
La malaria è clinicamente una malattia di difficile interpretazione in quanto si manifesta in molti modo diversi, spesso non viene riconosciuta, talvolta sottovalutata dai viaggiatori sia per brevi periodi che per lunghi viaggi.
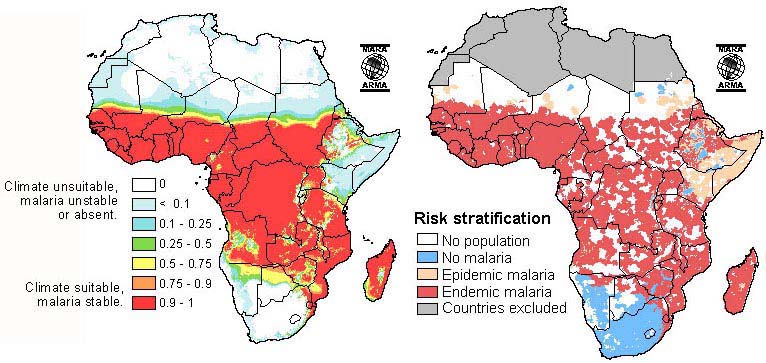
Il 90% dei casi si verificano nell’Africa subsahariana e quasi tutti i casi di decesso sono dovuti al Plasmodium falciparum. In Africa la malattia è la prima causa di morte; la maggior parte degli altri casi di infezione si verificano nel sud-est asiatico, in Oceania e in America Latina. Di solito il rischio è a una altitudine inferiore ai 1500m s.l.m., ma con condizioni climatiche favorevole ci può essere rischio sino a 3000m s.l.m.
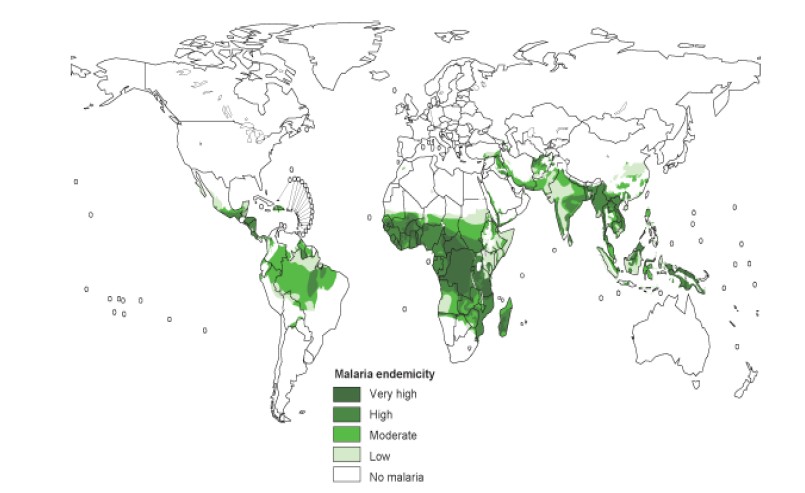
I casi in Europa sono tutti di importazione, cioè il contagio è avvenuto nei paesi dove è presente la malattia e non si trasmette da persona a persona nel nostro continente. Raramente si è verificato qualche caso autoctono, cioè la malattia si è manifestata in persone che non avevano viaggiato in territori endemici. Questi casi si erano manifestati dopo puntura di zanzare che erano state trasportate da aeroplani (malaria degli aeroporti). Bisogna considerare la possibilità di contagio da zanzara importata attraverso i mezzi di trasporto quali navi ed aerei.
Eziologia
L’agente infettivo è un parassita, monocellulare, del genere Plasmodio. Esistono 4tipi di plasmodio: falciparum, vivax, ovale e malariae.
Ciclo vitale.
Gli sporozoiti sono la forma infettante del plasmodio e vengono inoculati nell’ospite dalla puntura della zanzara femmina del genere Anopheles. Dopo una breve permanenza nel circolo ematico, gli sporozoiti invadono le cellule del fegato (ciclo esoeritrocitario); si ha il primo ciclo di moltiplicazione asessuata con produzione di schizonte, plurinucleato, che rompendosi libera nel sangue nuovi merozoiti mononucleati, che infettano i globuli rossi (ciclo eritrocitario). All’interno del globulo rosso avviene il secondo ciclo asessuato: il merozoite si muta in trofozoite, poi in schizonte per produrre altri merozoiti (dai 6 ai 36 per ogni schizonte) che rompono i globuli rossi, infettandone altri e cosi si ripete il ciclo.
A seconda del plasmodio infettante il ciclo si ripete ad intervalli regolari: ogni 48 ore per P. falciparum, P. vivax e P. ovale, e ogni 72 ore per P. malariae.
Se l’infezione è dovuta a P. vivax e P. ovale alcuni degli sporozoiti possono persistere quiescienti nelle cellule epatiche: ipnozoiti (forme “dormienti”), e riattivandosi ciclicamente possono dare ricadute anche dopo settimane e mesi dopo la prima infezione Dopo vari cicli alcuni trofozoiti si differenziano in forme eritrocitarie sessuate, i gametociti; sono queste le forme che permettono il mantenimento del ciclo del plasmodio nell’ambiente: l’uomo è il serbatoio dei gametociti da dove pescano le zanzare. Il microgametocita “maschio” ed il macrogametocita “femmina” vengono ingeriti dalla zanzara quando questa punge l’individuo infettato. Il ciclo sessuato nella zanzara è detto sporogonico. Nello stomaco dell’insetto, i gametociti escono dal globulo rosso che li ospita: subiscono diverse trasformazioni sino a che un flagellato (microgametocita maschio) feconda una macrogametocita femmina generando lo zigote. Lo Zigote cresce di misura, raggiunge l’intestino della zanzara dove diventa ovocisti, che si rompe liberando sporozoiti che raggiungono le ghiandole salivari della zanzara, pronta a trasmettere il plasmodio al altro individuo.
Il maschio della zanzara non punge
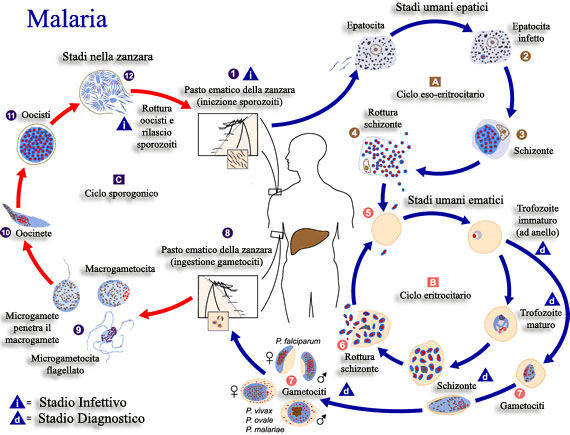
fonte: http://www.dpd.cdc.gov/DPDx/HTML/Malaria.htm
Incubazione
L’incubazione varia a seconda del plasmodio coinvolto:
P.Falciparum 7-14 giorni
P.Vivax e Ovale 8-14 giorni
P.Malariae 7-30 giorni
In alcuni casi di infezione con P.vivax e P.ovale, l’incubazione può essere di 8-10 mesi
Sintomi.
La sintomatologia è aspecifica, il più delle volte si presenta come una sindrome simil influenzale, dopo il periodo di incubazione. La febbre c’è sempre, può essere una febbre “ciclica”, accompagnata da tremori e sudorazione, anche se no è da considerasi la regola che la febbre sia ciclica, anzi il più delle volte non è così. La ciclicità della febbre è legata alla specie del parassita coinvolto, si manifesta con la rottura dei globuli rossi (ciclo eritrocitario)
Nel caso del P.Falciparum è ogni 48h (terzana maligna), l’infezione presenta accessi febbrili ogni 48 ore, ma la febbre è spesso irregolare e può anche ricomparire ogni giorno. Comporta un’anemia piuttosto intensa, con grave deperimento organico, e se non ben trattata ha esito letale.
Anche nel caso di infezione con P.Vivax ed Ovale il rialzo termico compare ogni 48h, ma è meno intensa (terzana benigna), puo’ avere spontaneamente una durata di un paio di anni, e tende a recidivare con facilità (ipnozoiti epatici)
In caso l’infezione sia dovuta a P.malariae, gli attacchi febbrili si ripetono ogni 72h (malaria quartana) (1 giorno febbre, 2 di non febbre ed 1di febbre), tende a persistere molto a lungo e a recidivare
La febbre può essere accompagnata da altri sintomi quali mal di testa, dolori muscolari e debolezza, vomito, diarrea, tosse, mentre in altre occasioni la malaria non si presenta con le tipiche febbri cicliche, ma è quasi costante la cefalea nucale, i brividi, e l’alternanza del caldo e del freddo, con un malessere ingravescente.
La distruzione dei globuli rossi provoca anemia.
Le infezioni non trattate o trattate in modo inadeguato possono provocare insufficienza renale, edema polmonare, ipertensione endocranica con coma e giungere all’exitus. La morte è provocata dall’impilamento delle cellule parassitate nel microcircolo di diversi organi vitali, in particolare nella circolazione cerebrale (malaria cerebrale solo per P falciparum), provocando un vero e proprio ostacolo al sangue, i globuli rossi si agglutinano e mancando l’ossigenazione a tali organi, questi vengono danneggiati irreversibilmente anche in sole 24ore dall’infezione.
L’attacco malarico dura circa 8-14 ore, inizia con uno stadio caratterizzato da sensazione di freddo “brividi scuotenti”, seguito dal rialzo termico solitamente elevato (40°C). A questa prima fase segue una seconda in cui il malato prova la sensazione di caldo, accompagnata a dolori al capo, nausea, vomito, dolori addominali diffusi. L’attacco termina con la sudorazione profusa e l’abbassamento della temperatura corporea. Il paziente alla fine è seriamente provato fisicamente.
Le donne in stato di gravidanza sono la preda più facile della malaria. L’indebolimento del sistema immunitario durante la gravidanza rende l’infezione più probabile, e l’anemia abituale in gravidanza dà al parassita un “mortale” vantaggio. Queste donne hanno quattro volte di più la probabilità di ammalarsi e la metà delle probabilità di sopravvivere alla malaria cerebrale; se sopravvivono spesso il feto muore perché i farmaci e la febbre spesso provocano l’aborto spontaneo. L’OMS (Organizzazione Mondiale della Sanità) consiglia alle donne in gravidanza di non andare in vacanza in aree in cui ci sia trasmissione di P. falciparum clorochino-resistente
Spesso compare la cosidetta Hypereactive Malarial Splenomegaly (HMS): splenomegalia malarica iperreattiva, in passato “Sindrome splenomegalica tropicale” è una condizione patologica conseguente a una risposta immunologica aberrante nei confronti di un’infezione malarica, che si manifesta con severa splenomegalia (aumento di volume della milza) in ragazzi o adulti, alti livelli di anticorpi anti-Plasmodium. L’ipersplenismo è responsabile dell’anemia emolitica cronica, della leucopenia e trombocitopenia (diminuzione dei glubuli bianchi e delle piastrine). Si hanno calo ponderale, astenia,tachicardia, dispnea dopo sforzo, senso di peso e dolenzia a livello della milza.
I bambini sono considerati soggetti a rischio poiché possono sviluppare forme perniciose che conducono all’exitus in tempi molto brevi.
Immunità
Nelle aree endemiche, i ripetuti contagi, a cui una persona è soggetta, sviluppano un livello elevato di anticorpi, che permette una resistenza alle infezioni. Nella maggior parte dei casi questi soggetti sono asintomatici pur portando nelle proprie cellule il parassita (portatori sani dell’infezione). I soggetti non immuni, in zona endemica, possono ammalarsi molto più facilmente di un soggetto considerato immune, e possono avere forme di malattie più gravi.
I bambini nati in area endemica sono protetti per i primi 6 mesi dall’immunità passiva materna, data dagli anticorpi ereditati dalla madre, poi si ha una progressiva acquisizione di una “semi-immunità”, per successive esposizioni alle infezioni del plasmodio. Si hanno ricorrenti attacchi di malaria, dall’età di pochi mesi fino a 5-10 anni, prima di raggiungere uno stato di semi-immunità. Molti bimbi soffrono di ritardo di crescita e altri muoiono. Se i bimbi sopravvivono, mantengono la semi-immunità per continue reinfezioni, per tutta la vita, finché risiedono in area endemica. La semi-immunità può calare temporaneamente durante la gravidanza, e si attenua col tempo negli individui che abbandonano le zone endemiche (scompare dopo 2 anni di distanza).
Diagnosi
Può essere fatta in diverse modalità
Microscopia: esame stircio o goccia spessa,
QBCTM quantitative buffy coat method
Immonologici: IFI test, immunoflorescenza indiretta
altri test si basano sulla cattura della proteina II (PfHRP-II)
Studio attività enzimatiche: Determinazione dell’antigene (histidine rich protein-2, HRP-2) associato con il parassita della malaria (P. falciparum e P. vivax)
Determinazione dell’enzima lattato deidrogenasi del Plasmodio (pLDH) sia mediante la sua attività enzimatica che mediante immunoassa
Tecniche di biologia molecolare: PCR
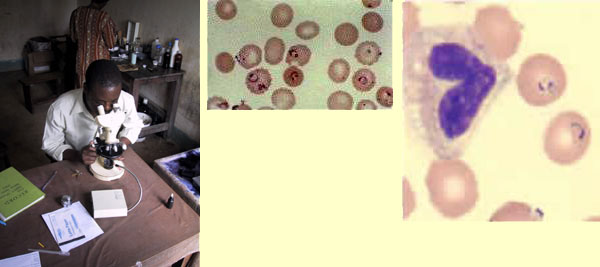
Esiste anche la possibilità di farsi una autodiagnosi con dei test a cartina; è necessario procurarsi una goccia di sangue del paziente infetto, farla cadere su di una apposita striscia, aspettare qualche minuto e confrontare il risultato del test con la legenda. Ne esistono in commercio diversi tipi, ma tutti funzionano con la stessa modalità della goccia di sangue.
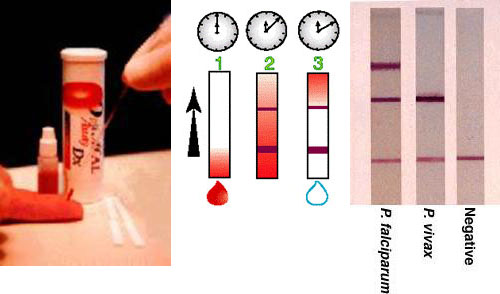
Fonte: http://www.malariatest.com/index.html
Questi test hanno dei limiti soprattutto nelle infezioni miste, diversi autori hanno sempre dubitato di tali test, ma anche in questo campo la tecnologia fa passi avanti.
Ad esempio il nuovo NOW® Malaria è un test rapido immunocromatografico, per la ricerca dell’antigene specifico del Plasmodium falciparum ed un antigene che è comune a tutte e quattro le specie conosciute di malaria, nel sangue intero. Il test usa due anticorpi che sono fissati in due diverse bande nella zona di lettura della striscia. Un anticorpo è specifico per l’antigene HRPII (Proteina ricca d’istidina). Tipico per il P. falciparum. L’altro anticorpo è specifico per un antigene che è comune a tutti e 4 i plasmodi.
Per ottenere sangue capillare, è necessario pungere con una lancetta sterile il polpastrello, il tallone o altro luogo adatto, pulire ed asciugare la zona con un tampone sterile. Se si usa la lancetta o un pungidito per perforare la pelle, raccogliere il sangue direttamente nel tubo capillare. Riempire l’intero tubo capillare di sangue ed usarlo immediatamente.
Raccogliere il sangue venoso, in una provetta con EDTA. Se il test non può essere eseguito immediatamente, il sangue può essere conservato in frigo per tre giorni a 2° – 8° C. Questo test ha raggiunto una sensibilità del 93% nella diagnosi della malaria, sino al 99-100% per la malaria da P.falciparum, mentre scende al 89% per la malaria da P.vivax, mentre una specificità del 96% per P.falciparum e 98% per P.vivax.
Un recente studio eseguito dalla Fondazione IRCCS Policlinico San Matteo di Pavia “Comparison of three diagnostic techniques for malaria: a rapid diagnostic test (NOW((R)) Malaria), PCR and microscopy ; Gatti S, Gramegna M. Bisoffi Z et all, Ann Trop Med Parasitol. 2007 Apr;101(3):195-204” ha verificato i risultati del test con l’esame classico in laboratorio grazie alla microscopia, concludendo che se pur il test è molto attendibile per la diagnosi di malaria da P.falciparum, ci sono ancora dei dubbi sulle infezioni miste, e pertanto non può sostituire il classico esame con microscopio ai fini diagnostici.
Controllo e Prevenzione
Le attuali strategie di controllo di Roll Bach Malaria http://www.rollbackmalaria.org/ si concentrano in 5 punti fondamentali
1. Rapida diagnosi e trattamento della malaria con farmaci efficaci
2. Prevenzione della malattia mediante l’utilizzo di insetticidi e la bonifica di terreni
3. Prevenzione della malaria per le donne in gravidanza
4. Continua sorveglianza dell’insorgere di epidemie per realizzare una rapida risposta
5. Programmi di educazione
Prevenzione meccanica
La prima precauzione contro la malaria è la prevenzione contro le punture delle zanzare. Questa si può attuare mediante una serie di abitudini comportamentali (alla sera e al mattino indossare indumenti ampi che giungano a coprire polsi e caviglie; adottare l’impiego di zanzariere che avvolgono il letto durante la notte, meglio se impregnate di insetticida) o mediante l’uso di presidi chimici (repellenti ad uso cutaneo, uso di spirali zanzarifughe al piretro, uso di altri piretroidi di sintesi e mediante fornelletti elettrici)
La zanzara femmina di Anopheles, vettore del parassita malarico, usa stimoli termici ed olfattori, ma anche visivi, per localizzare l’ospite da pungere per realizzare il suo pasto; in particolare viene attratta da concentrazioni di anidride carbonica. I colori scuri attirano l’insetto in questione che usa pungere al tramonto e durante le prime ore della notte, meglio abiti lunghi e di colore bianco o chiaro; l’aria condizionata diminuisce notevolmente il rischio di punture di insetti.
I repellenti sono sostanze chimiche che allontanano l’insetto. La maggior parte dei repellenti contiene DEET (N,N-diethyl-methyl-toluomide) sostanza molto attiva in uso da oltre 40 anni. E’ in commercio con concentrazioni variabili tra il 7 ed il 20%; le prime più adatte ai bambini. La maggiore o minore concentrazione non influisce sulla attività ma sulla durata d’azione (in media 2-3 ore). Va usato con cautela in gravidanza, il prodotto attraversa la placenta, e la sua sicurezza in gravidanza no è stata del tutto accertata. Un importante studio ha testato il DEET in donne al secondo e terzo trimestre di gravidanza, non si sono registrati eventi avversi nelle donne e ne nei bambini controllati sono all’anno di età. Il prodotto può danneggiare la plastica (attenzione ad occhiali, orologio ecc.), il rayon ed il cuoio, mentre non intacca cotone, nylon e lana.
Recentemente è stato messo in commercio il Bayrepel (acido 1-pipetidincarbossilico, 2-(2-idrossietil)-,1-metilpropilestere) di pari efficacia al DEET, no danneggia gli oggetti in plastica e tessuti sintetici; è raccomandato dal World Health Organization (Report of the fourth WHOPES Working Group Meeting, WHO/CDS/WHOPES/2001.2 Geneva: WHO, 2001) autorizzato dai 2 anni di età.
Altri repellenti sintetici sono attivi per circa 3-4 ore e vanno applicati periodicamente (ogni 3 ore circa) durante esposizione a rischio. I repellenti non devono essere inalati o ingeriti e sono pericolosi su pelli irritate o sugli occhi . Vanno usati con prudenza nei bambini e mai applicati sulle loro mani perché facili strumenti di contaminazione degli occhi e della bocca. Il repellente va applicato su tutta la parte del corpo scoperta: è provato che le zanzare possano pungere a meno di un centimetro da una zona coperta. Vanno evitati nei bimbi inferiori ad un anno di età nelle donne in stato di gravidanza, e se si permane a lungo in zona endemica, per il pericolo di tossicità.
Per eliminare gli insetti si usano gli insetticidi, sostanze che attaccano il sistema nervoso dell’insetto uccidendolo.
Ne esistono di sintetici, a base di piretroidi, e naturali a base di piretro (ottenuto dai fiori di crisantenum cineraricefolium); quest’ultimo puo’ essere anche usato come repellente.
La permetrina e la deltametrina contenuti in molti insetticidi sintetici, sono prodotti considerati poco tossici per i soggetti adulti e quindi possono essere utilizzati negli ambienti chiusi anche in presenza di bambini piccoli al di sotto dei due anni di età. Impregnare i vestiti e le zanzariere con gli insetticidi aiuta a ridurre il rischio di contagio. Il suo impiego sulla pelle è registrato soltanto per il trattamento della scabbia, mentre non lo è il suo uso come repellente. La permetrina è disponibile presso alcuni negozi con il nome di Duranon o Permanone sia in forma liquida sia in forma spray. Una confezione spray da 170 grammi può essere sufficiente per trattare due cambi di indumenti
“Prima del viaggio stendere i vestiti che si pensa di indossare, si irrora di insetticida sino ad inumidirli li si rivolta e li si irrora nuovamente quindi li si lascia asciugare. La permetrina così applicata resiste a diversi successivi lavaggi ed i vestiti rimangono impregnati fino a 2-6 settimane. Le zanzariere dovrebbero essere trattate mensilmente per mantenere la loro efficacia”
I dispositivi elettronici ad ultrasuoni non sono efficaci, cosi come l’assunzione di aglio e vitamine del gruppo B.
Chemioprofilassi
La profilassi farmacologica ha lo scopo di uccidere il parassita già inoculato nell’individuo, prima che il plasmodio inizi il suo ciclo vitale nel sangue; si base sul principio secondo il quale si raggiunge e si mantiene una concentrazione plasmatica di un farmaco antimalarico a livelli bassi per essere curativi, ma sufficienti a impedire che si sviluppi la malattia dopo la puntura della zanzara; questa concentrazione deve essere mantenuta per tutto il periodo in cui si è potenzialmente esposti alla malattia.
In commercio esistono diversi farmaci, e per tutti vige la norma che devono essere prescritti da un medico, ma prima di adottarne uno è bene farsi visitare da un medico esperto in medicina tropicale, o un medico che conosce la materia, infatti la chemioprofilassi può differire non solo dalla zona endemica in cui ci si reca, ma anche da individuo ad individuo a seconda di condizioni morbose concomitanti e preesistenti, o a secondo del peso. Alcuni antimalarici presentano delle controindicazioni, il medico ne dovra’ tener conto per ridurre gli effetti collaterale e rendere la profilassi il piu’ efficace possibile; pertanto la terapia sara’ personale.
E’ bene tenere conto che nessun farmaco antimalarico fornisce una protezione completa.
Di seguito verranno elencati i farmaci per la profilassi antimalarica con il dosaggio riportato in scheda tecnica.
Clorochina. Clorochina Bayer®,
N° di autorizzazione all’immissione in commercio: AIC n. 00836615 dal gennaio 1953, rinnovata: agosto 1998
Modalità di assunzione: il farmaco deve essere assunto una volta alla settimana, cominciando la settimana prima di giungere nella zona endemica, continuando la somministrazione per tutta la durata del soggiorno nella zona endemica e continuando per 4 settimane dopo il rientro dalla zona malarica.
Indicazioni: solo per P. falciparum sensibile alla clorochina, o nei paesi dove ci sia solo il P.vivax. Non protegge dagli ipnozoiti epatici da vivax
Principali eventi avversi: Prurito nelle persone di colore, nausea, cefalea, eruzioni cutanee, alterazioni delle unghie, opacità corneale reversibile, fotofobia, retinopatia, discrasie ematiche, psicosi, convulsioni, alopecia, reazioni cardiovascolari, ipotensione arteriosa. Puo’ ridurre la risposta anticorpale da parte dell’organismo a vaccinazioni somministrate in concomitanza o poco prima. Non somministrare in soggetti affetti da psoriasi, porfirie, epilessia, gravi nefropatie ed epatopatie, o deficit dell’enzima G6PD.
Posologia per profilassi: 5mg di sostanza base per ogni kg di peso alla settimana (le cp della clorochina attualmente in commercio sono da 250mg ma contengono 150mg di sostanza base)
kg 9-16 45-80mg la settimana = 1/3 – ½ cp
kg17-14 85-120mg la settimana = ½ – ¾ cp
kg25-35 120-175mg la settimana = ¾ – 1 cp
kg 35-50 175-250mg la settimana = 1 ¼ – 2 cp
kg>50 250mg la settimana = 2cp
Proguanile Plaquenil®, Paludrine®
N° di autorizzazione all’immissione in commercio:AIC n. 028278012 del giugno 1992, rinnovata: gennaio 1997
Modalita’ di assunzione: il farmaco deve essere assunto tutti i giorni, cominciando il giorno prima di giungere nella zona endemica, continuando la somministrazione per tutta la durata del soggiorno nella zona endemica e continuando per 4 settimane dopo il rientro dalla zona malarica.
Indicazione: il farmaco da solo non e’ attivo, in associazione con la clorochina ha una efficacia del 70% contro P.falciparum in zone colorochina resistenti.
Principali eventi avversi: anoressia, ulcere cavo orale, nausea, interferisce con il vaccino antitifico. Controindicato negli individui con disfunzioni epatiche e renali, alterazioni retiniche
Posologia per profilassi: 3mg di sostanza base per ogni kg di peso al giorno (le cp in attualmente in commercio sono da 100mg)
kg 9-16 25-50mg die = ¼ – ½ cp
kg17-14 50-75mg die = ½ – ¾ cp
kg25-35 75-100mg die = ¾ – 1 cp
kg 35-50 100-150mg die = 1 – 1 ½ cp
kg>50 200mg die = 2cp
In commercio esiste gia’ l’associazione clorochina+proguanile con il nome commerciale di Savarine®, le compresse contengone 100mg di clorochina +200 di proguanil, la posologia per un adulto e’ di 1cp al giorno, non e’ riportata la posologia per individui sotto i 50kg. La modalita’ di assunzione e’ come sopra, 1cp al giorno, dal giorno prima di raggiungere la zona endemica e per 4 settimane dopo il rientro dalla stessa. Gli eventi avversi sono gli stessi della clorochina e del proguanile.
Meflochina Lariam®, Mephaquine®
N° di autorizzazione all’immissione in commercio: AIC n 027250024 rinnovata nel giugno 2000
Modalità di assunzione: il farmaco deve essere assunto una volta alla settimana, cominciando la settimana prima di giungere nella zona endemica (anche se alcuni autori consigliano 2-3 settimane prima), continuando la somministrazione per tutta la durata del soggiorno nella zona endemica e continuando per 4 settimane dopo il rientro dalla zona malarica.
Indicazioni: per P. falciparum in zone resistenti alla clorochina. Non protegge dagli ipnozoiti da P. vivax; effecacia oltre il 90%
Principali eventi avversi: vertigini, nausea, cefalea, incubi, irritabilita’,insonnia, alterazione dell’umore, ansia, convulsioni, psicosi. Controindicato in pazienti con psicosi, anche depressioni ed altri disturbi dell’umore, epilettici, piloti e operatori di macchine operatrici. La meflochina influisce sulla risposta anticorpale di alcuni vaccini,
Posologia per profilassi: 5mg prokg la settimana. Le compresse in commercio contengono 250mg di principio attivo
kg<5 non raccomandato
kg 7-8 35-40 mg la settimana
kg9-12 45-60 mg la settimana
kg13-16 65-80 mg la settimana = ¼ -1/3 cp
kg17-24 85-120mg la settimana = 1/3 – ½ cp
kg25-35 125-175mg la settimana = ½ – ¾ cp
kg35-50 180-250mg la settimana = ¾ – 1 cp
kg>50 250mg la settimana = 1cp
Doxiciclina Bassado®, Vibramicina®
N° di autorizzazione all’immissione in commercio: AIC n.021635065 del novembre 1969, revisione del giugno 2002
Modalita’ di assunzione: il farmaco deve essere assunto tutti i giorni, cominciando il giorno prima di giungere nella zona endemica, continuando la somministrazione per tutta la durata del soggiorno nella zona endemica e continuando per 4 settimane dopo il rientro dalla zona malarica. Non superare i 3mesi di trattamento.
Indicazione: Indicata in caso di soggiorno in zona endemica ad alto rischio dove esista P.falciparum resistente alla meflochina; indicata anche in soggetti che non possono assumere la meflochina ed altri farmaci in zone di forte resistenza alla clorochina. Effecacia oltre il 90%
Principali eventi avversi: Disturbi gastrointestinali, candidiasi vaginale, fotosensibilità, reazioni allergiche, alterazioni dell’emocromo, alterazioni renali, epatite. Controindicato in bambini sotto 12anni di eta’, non somministrare in gravidanza, non associare agli antiacidi, in paziente con allergie alle tetracicline, in soggetti con disfunzioni epatiche
Posologia per profilassi: 1,5mg pro kg al giorno. Le compresse sono di 100mg
kg<25kg non raccomandato
kg25-35 40-50mg die = 1/3 – ½ cp
kg36-50 50-100mg die = ½ – 1 cp
kg>50 100mg die = 1cp
Atovaquone+proguanile Malarone®
N° di autorizzazione all’immissione in commercio: AIC n 033299013/M del 8/luglio 1997, revisione il 17 gennaio 2002, in commercio in Italia dal 5 dicembre 2003
Modalita’ di assunzione: il farmaco deve essere assunto tutti i giorni con il cibo a bevande a base di latte per favorire l’asorbimento, cominciando il giorno prima di giungere nella zona endemica, continuando la somministrazione per tutta la durata del soggiorno nella zona endemica e continuando per 1 settimane dopo il rientro dalla zona malarica. Avvertenze: se si vomita entro 1ora dalla assunzione è necessario riassumere la dose
Indicazione: rappresenta una alternativa ai chemioterapici per zone colorochinoresistenti. Sia per profilassi che per il trattamento della malaria a dosaggi diversi. Non protegge dagli ipnozoiti epatici da P.vivax; efficacia del 96%
Principali eventi avversi: nusea, vomito, dolori addominali, diarrea, esantema, convulsioni, cefalea insonnia. Controindicato in pazienti con problemi renali, insufficienza renale (clerance creatinina < 30ml/min) i suoi livelli plasmatici si riducono se si e’ in trattamento con alcuni antibiotici (rifampicina, tetracicline)
Posologia per profilassi: 1,5mg pro kg al giorno, le compresse in commercio contengono atovaquone 250mg e proguanile 100mg, disponibili anche la formulazione pediatrica con atovaquone 62,5mg e proguanile 25mg.
Kg<11 non raccomadato
kg11-20 ¼ cp/die adulto 1cp/die pediatrica
kg21-30 ½ cp/die adulto 2cp/die pediatrica
kg31-40 ¾ cp/die adulto 3cp/die pediatrica
kg>40 1 cp/die adulto ////
Ma qual è l’antimalarico più efficace e con minor effetti collaterali?
Impossibile dare una risposta, in gioco ci sono molte variabili da tenere in considerazione, sia individuali che ambientali; ricordatevi che nessun farmaco antimalarico fornisce una protezione completa; in letteratura la maggior parte degli autori è concorde che la terapia deve essere personale per ogni individuo e variabile a seconda dall’area endemica. L’Organizzazione Mondiale della Sanità (OMS o WHO) ha diviso le aree endemiche in 4 zone a cui è necessario applicare 4 gradi di protezione:

fonte: www.who.com
Le aree endemiche dell’Africa, secondo l’OMS, hanno un rischio tipo 4, quindi in tali casi sono consigliati solo 3 antimalarici oltre alla profilassi meccanica.
Dai dati dei diversi studi, sembra che la maggior parte dei viaggiatori che contraggono la malaria, non hanno fatto alcuna profilassi, o l’hanno abbandonata; il timore degli effetti collaterali è la causa principale, seguita dalla convinzione, senza cognizione di causa, che le dosi non fossero tutte necessarie, specialmente una volta ritornati a casa, considerano il pericolo di infettarsi scongiurato, interrompono la terapia senza tenere conto del periodo di incubazione della malaria.
Un’interessante ricerca eseguita dal Servizio di riferimento Regionale di Epidemiologia per la sorveglianza, la prevenzione e il controllo delle Malattie Infettive – SeREMI in Piemonte ha dato i seguenti risultati.
Chemioprofilassi effettuata in casi di malaria per anno di notifica in Piemonte.
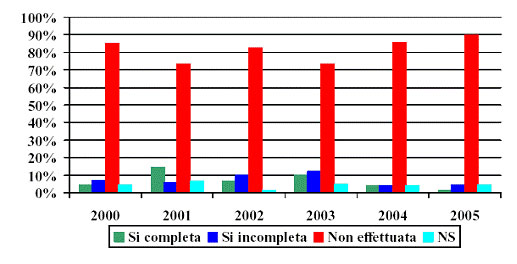
Perchè non ha fatto la chemioprofilassi o l’ha abbandonata?
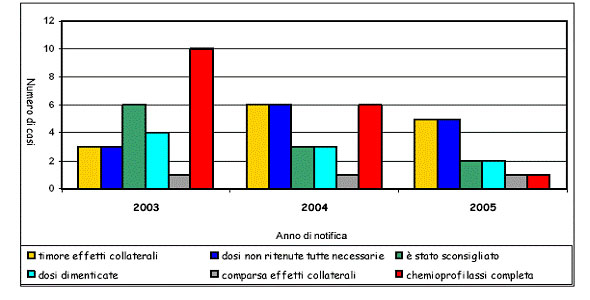
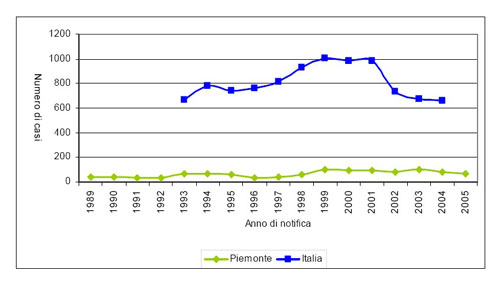
Anche la profilassi meccanica è spesso trascurata, questo quello che è emerso in Piemonte:
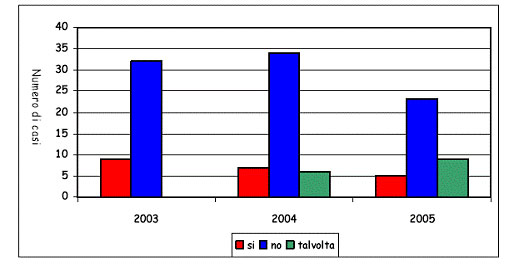
Numero di casi di malaria in Italia e Piemonte per anno di notifica.
In zone dove il rischio è di tipo 4 l’OMS, dei 3 chemioterapici disponibili non si sbilancia, non consiglia uno rispetto ad un altro…..mentre in letteratura sono diversi gli studi dove si considera il Malarone oltre che piu’ efficace, anche con minor effetti collaterali rispetto al Lariam, soprattutto gli effetti collaterali neuropsichiatrici, tando che iniziano a comparire studi a lungo termine, eseguiti in lavoratori per lunghi periodi in zona endemica. L’efficacia del Malarone e la minor incidenza di effetti collaterali lo fanno anche preferire rispetto al Savarine, che comunque viene escluso per le zone a rischio tipo 4, ma spesso viene impropriamente consigliato.
Il Malarone in Europa sino ad ora ha ottenuto la registrazione del farmaco per un periodo di somministrazione limitato, variabile da 28giorni a 3mesi a seconda dei paesi, mentre in USA la restrizione non e’ stata applicata. Questa differenza e’ dovuta al fatto che al momento della registrazione del farmaco non vi erano studi per profilassi a lungo periodo. Attualmente in letteratura scientifica ci sono studi dove si è testato il Malarone per periodi di 34settimane, ottenendo risultati molto positivi.
Riguardo alla doxicilina, le notizie sono contrastanti; l’efficacia del farmaco sembra essere buona, mentre la tollerabilità nei viaggiatori sembra essere inferiore addirittura al Lariam se fatta a lungo periodo.
La maggior parte degli studi a lungo termine sono stati eseguiti in militari europei in missione in zone endemiche; un recente studio, eseguito su 1400 militari turchi in missione in Afghanistan ha dimostrato la migliore tollerabilità del Lariam rispetto alla doxiciclina, la profilassi è stata di 12 settimane, nessun militare ha contratto la malaria, nessun effetto collaterale pesante tanto da abbandonare la profilassi. Anche i militari australiani sembrano gradire il Lariam rispetto alla doxicilina, sia per il minori effetti collaterali (i più lamentano sintomi gastrointestinali per la doxiciclina) che per via della somministrazione settimanale invece che giornaliera.
Nella tabella sotto due importanti studi che paragonano gli effetti collaterali del Malarone rispetto a Lariam e Savarine.
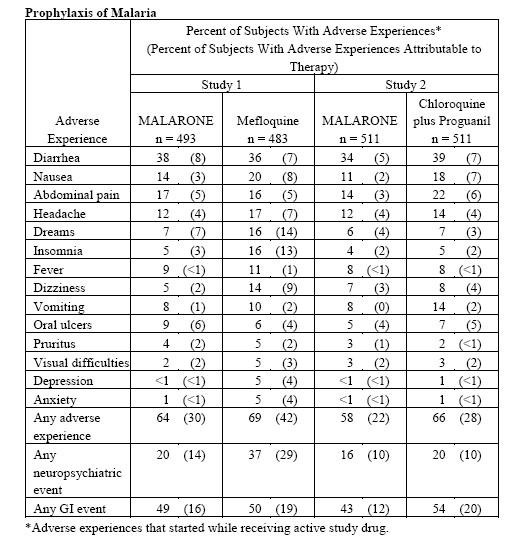
L’OMS raccomanda alle donne in stato di gravidanza di non recarsi in zona endemica, ma nelle popolazioni locali in zone endemiche si continua a morire di malaria, le donne gravide ed i loro bimbi in grembo sono le persone più a rischio con elevati tassi di mortalità. Le ricerche si stanno facendo, ma finora un farmaco sicuro come prevenzione per questi soggetti non si è trovato.
Riassumendo
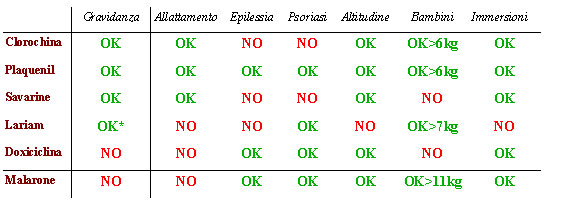
*non testato nel primo trimestre di gravidanza
Prima di intraprendere qualunque chemioprofilassi bisognerebbe conoscere la situazione attuale nel paese dove ci si intende recare, ogni anno viene pubblicato dal OMS il libro “International travel and health publication” dove è riportata la situazione di ogni paese, http://www.who.int/ith/countries/en/index.html se la zona è a rischio e di che grado, quindi recatevi da un medico esperto di medicina tropicale, e fatevi consigliare al meglio.
La vaccinazione
Il vaccino potrebbe essere l’arma che oggi manca per combattere la malaria là dove sono più sfavorevoli le condizioni ambientali e sociali: ma la sua messa a punto è resa particolarmente difficile dai diversi stadi di sviluppo del parassita, ciascuno con caratteristiche molecolari e biologiche diverse, a volte molto variabili. E’ come trovarsi di fronte, in pratica, a tre agenti patogeni diversi, senza sapere quale attaccare per bloccare l’infezione.
I primi tentativi di immunizzare contro la malaria risalgono agli anni sessanta, quando alcuni ricercatori avevano osservato gli effetti protettivi di plasmodi attenuati, provenienti da zanzare irradiate.
Ma il primo vero vaccino è stato messo a punto vent’anni dopo dal colombiano Manuel Patarroyo, che ha utilizzato un cocktail di peptidi sintetici corrispondenti a proteine espresse dal parassita in varie fasi della sua maturazione. I primi risultati nelle scimmie avevano acceso molte speranze, anche se il modo di procedere del ricercatore, ritenuto troppo grossolano, aveva suscitato molte critiche. Passando all’uomo, però, gli entusiasmi si sono presto raffreddati: in Africa il vaccino è risultato assai poco protettivo, e nell’ultimo studio, condotto in un campo profughi della Thailandia e terminato nel 1995, la sua efficacia appariva praticamente nulla. D’altra parte l’OMS aveva già ritenuto il vaccino insufficiente, sospendendo le sperimentazioni su vasta scala.
Gli studi sono tuttavia continuati, e proprio all’inizio di quest’anno si sono avuti i primi positivi riscontri di un altro vaccino, sviluppato dal Walter Reed Army Institute in collaborazione con la SmithKline Beecham Biologicals. “E’ il primo vaccino ottenuto grazie alla clonazione dei geni del plasmodio” dice José Stoute, uno dei ricercatori impegnati nel progetto. “Si basa su un solo antigene superficiale dello sporozoita, la proteina circumsporozoita, che viene iniettata in associazione con composti immunostimolanti per potenziare la risposta immunitaria”. Anche se deve ancora essere valutato nelle zone endemiche, rappresenta un notevole progresso, perché dimostra che l’immunizzazione contro un singolo antigene sporozoitico è in grado di arginare l’infezione, e sottolinea il ruolo degli adiuvanti immunologici.
A questo punto ai ricercatori si aprono molte strade: tutte le fasi di sviluppo del parassita possono infatti diventare bersaglio della risposta immunitaria, e le tecniche per costruire e potenziare un vaccino sono sempre più numerose e sofisticate.
Alcuni dei vaccini in fase di studio sono indirizzati, come quello di Patarroyo, contro i plasmodi che si trovano nei globuli rossi; non bloccano l’infezione, ma dovrebbero essere capaci di prevenire i sintomi. Uno dei più studiati si basa su una proteina di superficie dei merozoiti (MSP1), che ha dimostrato di conferire protezione ad alcuni animali, e non presenta – caratteristica preziosa – variazioni antigeniche.
Altri tentativi si rivolgono verso i gameti del parassita: sono i cosiddetti “vaccini altruistici”, che non hanno effetti sulle persone vaccinate, ma interrompono la trasmissione del plasmodio agendo contro i gameti nell’intestino della zanzara. Un sistema molto usato è quello di potenziare i vaccini con adiuvanti immunologici: appare promettente l’impiego di liposfere biodegradabili, cioè di piccolissime vescicole lipidiche che contengono al loro interno l’antigene. Oltre a costituire un ottimo veicolo per il rilascio controllato del materiale antigenico, potenziano la risposta immunitaria perché fungono da adiuvanti e presentano in modo ottimale gli antigeni ai macrofagi.
Ma l’approccio più rivoluzionario è rappresentato dai vaccini a DNA. Anziché immettere l’agente patogeno, o una parte di esso, in forma attenuata, per suscitare la risposta immunitaria vengono introdotti suoi frammenti di DNA che codificano un determinato antigene. Inglobando i nuovi geni, le cellule del soggetto vaccinato acquisiscono la capacità di sintetizzare ex novo la proteina antigenica: l’organismo la riconoscerà come estranea e lancerà l’attacco immunitario, che risulterà indirizzato anche contro il vero antigene del microrganismo patogeno. Il soggetto sarà così immunizzato contro l’agente senza esserne venuto in contatto.
La genetica offre vantaggi sul piano dell’allestimento dei vaccini, della conduzione dei test e della produzione su larga scala; consente di eliminare le elaborate e costose procedure di controllo e purificazione dei vaccini tradizionali, annullando il pericolo di contaminazione e i rischi legati all’impiego di agenti patogeni vivi o attenuati.
Per questo i vaccini a DNA oggi allo studio sono parecchi: contro l’epatite B e C, contro l’HIV, la tubercolosi, l’influenza e diverse altre malattie virali e parassitarie, tra le quali non poteva mancare la malaria. “Di tutte le tecnologie disponibili, quella che prevede l’utilizzo di DNA sembra offrire i migliori presupposti per lo sviluppo di un vaccino contro le varie fasi del plasmodio, capace di indurre tanto una risposta immunitaria umorale quanto una risposta citotossica, entrambe ritenute indispensabili per contrastare l’infezione malarica” spiega Guido Grandi, responsabile del Dipartimento di biologia molecolare della Chiron Vaccines italiana. Si è visto infatti negli animali che mentre gli antigeni sintetizzati inducono la formazione di anticorpi, i frammenti di DNA che lavorano all’interno della cellula stimolano una reazione cellulomediata. L’azienda di Siena è impegnata anch’essa sul fronte della malaria, e sta cercando di sfruttare la possibilità di associare nello stesso vaccino più frammenti di DNA che codificano antigeni diversi. “Stiamo lavorando a un vaccino basato su un cocktail di cinque geni che codificano altrettanti antigeni appartenenti a vari stadi di sviluppo. Iniettato nel topo, determina una risposta anticorpale contro tutti gli antigeni utilizzati, e i test di immunofluorescenza dimostrano che gli anticorpi sono in grado di riconoscere le diverse fasi del plasmodio”.
Negli Stati Uniti è invece a buon punto il progetto, realizzato dal Naval Medical Research Institute, di un vaccino a DNA che codifica la proteina circumsporozoita del plasmodio; i risultati ottenuti nei roditori appaiono incoraggianti, tanto che la sperimentazione sull’uomo potrebbe cominciare entro l’anno.
“I geni sono introdotti sotto forma di plasmidi mediante una semplice iniezione muscolare: questo è sufficiente a far entrare il DNA nelle cellule dell’ospite, anche se sono poco chiari i meccanismi per cui ciò avviene”; commenta Grandi. L’utilizzo del “gene-gun”, la speciale arma che spara DNA nelle cellule, è ancora troppo complesso e impensabile su vasta scala. “La sicurezza di questi vaccini è garantita dal fatto che i frammenti di DNA estraneo non vengono integrati, come si potrebbe pensare, nel DNA delle cellule dell’ospite, ma rimangono isolati, in forma di episomi, così da poter essere degradati e scomparire dopo aver assolto al loro compito di esprimere l’antigene”.
Fonte http://www.stopmalaria.it
Trattamento della Malaria
Prima di tutto una premessa: l’individuo malato va ospedalizzato per il trattamento della malaria, per far fronte alle sue complicanze e per l’osservazione del paziente. Il viaggiatore si deve rendere conto che la malattia è grave, e nonostante i nuovi ritrovati, che il viaggiatore può facilmente recuperare sul mercato, l’ospedalizzazione va sempre fatta; ci si deve recare da un medico anche solo se nel sospetto di aver contratto la malattia, anche in loco.
Nonostante tale documento sia rivolto a personale non medico e non avendo la pretesa di essere una guida al trattamento, di seguito saranno trattati i diversi chemioterapici per combattere la malaria, al solo scopo informativo, tralasciando quello che è il supporto farmacologico delle complicanze, che appunto richiede l’ospedalizzazione e terapie somministrate da personale medico.
La prima raccomandazione arriva dall’OMS, che in base al parere di esperti internazionali, raccomanda l’introduzione di combinazioni di farmaci in sostituzione dei farmaci singoli (monoterapia) per la terapia della malaria…. L’OMS in particolare raccomanda l’utilizzo di combinazioni di farmaci che contengono composti dell’artemisinina, (ACT, artemisinin-based combination therapy).
La ACT è data dall’assozione di diversi farmaci, le principali associazioni sono:
Artemisina-lumefantrina
Artesunate-amodiaquine
Artesunate-meflochina
Artesunate-sulfadoxine-pyrimethamine
Arthemeter-artesunate
Artemisina/lumefantrina Riamet®, Coartem®
Non ancora commercializzato in Italia, Il Riamet si trova in Svizzera, Francia rilasciato dietro prescrizione medica, Il Coartem è lo stesso farmaco reperibile in Africa.
Il farmaco è una associazione di Artemisina 20mg, e Lumefantrina 120mg
Indicazione: Malaria da P.Falciparum, o infezioni miste da altri plasmodi, anche resistenze ad altri antimalarici.
Controindicazioni: Ipersensibilità ai componenti del prodotto. Gravidanza, fatta eccezione per casi di estrema gravità in cui il medico dovrà stabilire l’indicazione in funzione del contesto clinico. Non vi sono dati sull’impiego durante l’allattamento
Precauzioni: il farmaco non è stato studiato nei casi di malaria grave pertanto non ha indicazioni in questo caso. Il prodotto è assorbito meglio a stomaco pieno. In caso di intolleranza ai cibi assumere il farmaco con dei liquidi. In caso di vomito entro 1 ora dalla somministrazione ripetere la dose.
Molta cautela nell’impiego in soggetti con anomalie del ritmo cardiaco
Effetti Collaterali: Vertigini, stanchezza, alterazioni del sonno, cefalea, palpitazioni, dolori addominali, anoressia, nausea, vomito, diarrea, prurito, esantemi, tosse, artralgie e mialgie.
Posologia per il Trattamento
Il trattamento prevede 6 somministrazioni orali del farmaco al tempo 0 (diagnosi), dopo 8,24,36,60h con dosaggio a seconda del peso e quindi per età. Per adulti considerare oltre i 34Kg di peso
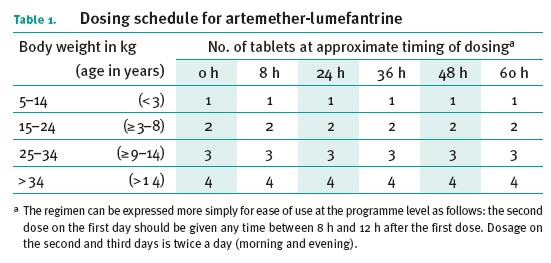
Artesunate-amodiaquine, Artesunate-sulfadoxine-pyrimethamine, Artesunate-meflochina . Artemal comb® Artemal complex®
Diverse associazioni di farmaci utilizzabili per il trattamento della malaria, utilizzabili al posto del Riamet
Posologia:
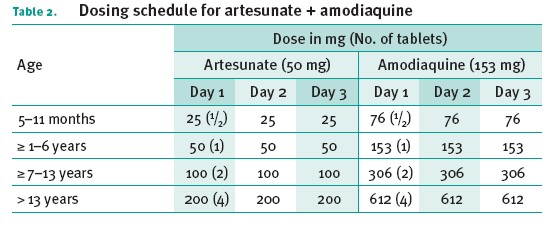
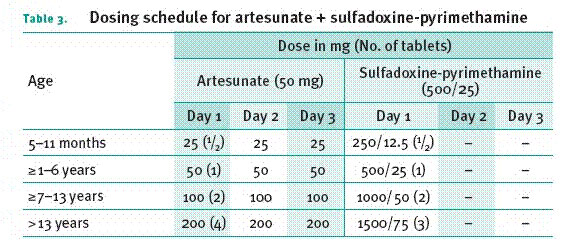
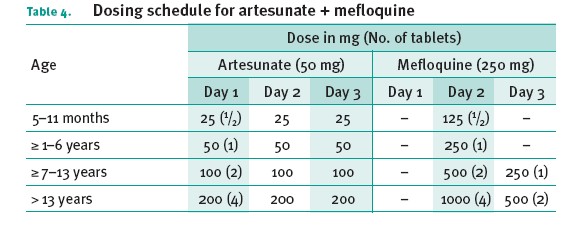
Arthemeter Paluther®, Artemether® altro farmaco per il trattamento, non si torva in Italia., non va usato da solo ma in associazione all’Artesunate Artemal®: 1cp due volte di per il primo giorno, quindi continuare con 1cp al di per 6giorni
Posologia per il Trattamento
Due sono i protocolli terapeutici, uno di 5 e l’altro di 3giorni
5giorni: 2flaconi intramuscolo (160mg) il primo giorno, quindi 1flacone intramuscolo al giorno (80mg) per 4giorni
3gironi: 2flaconi intramuscolo (160mg) al girono per 3giorni
Primachina
Usato solo per eradicare gli ipnozoiti (forme dormienti) nelle infezioni da Plasmodio vivax e ovale; alcuni degli sporozoiti possono persistere quiescienti nelle cellule epatiche e riattivandosi possono dare ricadute dopo la prima infezione, anche dopo settimane o mesi. Non viene usata per la profilassi
Controindicazioni: Deficit di G6PD, malattie sistemiche associate a granulocitopenia (per esempio artrite reumatoide, lupus eritematoso); gravidanza e allattamento, non testano nell’infanzia.
Effetti Collaterali: nuusea, vomito, anoressia, dolore addominale; meno spesso metaemoglobinemia, anemia emolitica in particolare in presenza di deficit di G6PD, leucopenia
Posologia per il Trattamento; Adiuvante in terapia con altro antimalarico in caso di sovrainfezioni di P.Vivax e Ovale
infezioni a Sud dell’Equatore: 0,5mg pro kg per 14giorni
infezioni a Nord dell’Equatore: 0,25mg pro kg per 14giorni
Alofrantrina Halfan® non in commercio in Italia È stata sviluppata dal “Walter Reed Army Institute of Research” (esercito degli USA) negli anni ’70.
Indicazione: trattamento della malaria non complicata da P.falciparum resistente alla clorochina
Controindicazioni: Gravidanza, allattamento; cardiopatie in genere; in particolare aritmie. Non associare alla meflochina.
Effetti Collaterali: Dolori addominali, disturbi gastrointestinali, cefalea, aumento transitorio degli enzimi epatici, tosse, prurito, anemia emolitica, convulsioni, aritmie cardiache (molto pericolose)
L’alofantrina è un farmaco che dovrebbe essere impiegato soltanto sotto controllo medico.
Sono possibili effetti collaterali anche gravi soprattutto del ritmo cardiaco. Non somministrare a pazienti che potrebbero avere turbe del ritmo cardiaco e a pazienti con deficit di tiamina. L’assunzione con i pasti ne aumenta l’assorbimento; se da un lato ciò potrebbe consentire un maggiore effetto, espone anche ad un maggior rischio di effetti collaterali.
Sulfadossina + Pirimetamina Fansidar®, Sulfalene + Pirimetamina Metakelfin®
Indicazioni: Farmaco raccomandato nei paesi in cui sia presente P.falciparum resistente alla clorochina e sensibile al sulfamidico; è segnalata resistenza alla combinazione sulfamidico + pirimetamina nelle seguenti regioni o paesi: bacino del Rio delle Amazzoni, Sud-Est asiatico, Africa (Kenia, Malawi, Tanzania, Uganda, Mozambico)
Controindicazioni Allergie ai sulfamidici ed alla pirimetamina; insufficienza renale grave, epatopatie gravi, discrasie ematiche. No ai bambini al di sotto di 1 mese; gravidanza; non va somministrata in caso di terapie recenti con la stessa combinazione o con altri inibitori del metabolismo dei folati (per esempio il Bactrim).
Effetti collaterali: Frequenti sono le reazioni cutanee eritematose, talora molto gravi, da ipersensibilità alla sulfadossina.
Posologia per il trattamento della malaria non complicata da P.Falciparum; 25mg pro kilo di sulfamidico in singola dose
<1anno di età: 0.25 cp in una volta
2tra 1-3 anni: 0.5 cp in una volta
tra 4-8 anni: 1 cp in una volta
tra 9-14 anni: 2 cp in una volta
adulti : 3cp die in una volta
Alcuni dei chemioterapici usati per la profilassi, a maggio dosaggio possono essere usati per la terapia, tra questi
Atovaquone+proguanile Malarone®
Indicazione: Malaria non complicata da P.falciparum resistente alla clorochina e ad altri antimalarici; informazioni limitate e quindi efficacia ancora da stabilire nelle altre infezioni malariche (P.vivax, P.malariae, P.ovale). Non indicato nei soggetti in profilassi con lo stesso Malarone®.
posologia per il trattamento della malaria non complicata da P.Falciparum
Kg<11 non raccomadato
kg11-20 1 cp/die adulto per 3giorni
kg21-30 2 cp/die adulto per 3giorni
kg31-40 3 cp/die adulto per 3giorni
kg>40 4 cp/die adulto per 3giorni
Clorochina. Clorochina Bayer®
Indicazioni: Malaria da P.falciparum sensibile alla clorochina; farmaco di scelta per le altre infezioni malariche (P.vivax, P.malariae, P.ovale).
posologia per il trattamento della malaria: 5mg di sostanza base per ogni kg di peso al giorno in 3 somministrazioni (le cp della clorochina attualmente in commercio sono da 250mg ma contengono 150mg di sostanza base). 600 mg (sostanza base) come prima dose al momento della diagnosi (4 compresse), seguite da 300 mg (due compresse) dopo 6 ore e quindi 300 mg al giorno (due compresse) nei due giorni successivi.
Doxiciclina Bassado®, Vibramicina®
posologia per il trattamento della malaria non complicata da P.Falciparum
il primo giorno 1dose ogni 12h, quindi 1dose al giorno per 6giorni
kg<25kg non raccomandato
kg25-35 = ½ cp a dose
kg36-50 = ¾ cp a dose
kg>50 = 1cp a dose
Meflochina Lariam®, Mephaquine®
posologia per il trattamento della malaria non complicata da P.Falciparum
25mg pro kg al giorno, frazionate in 3dosi giornaliere
<50kg 25 mg/kg in singola dose al momento della diagnosi
Per un adulto di oltre 50kg 1250 mg (5 compresse) al momento della diagnosi oppure 750 mg (3 compresse) al momento della diagnosi, 500 mg (due compresse) dopo 8 ore e 250 mg (1 compressa) dopo altre 8 ore.
Chinino
Non dimentichiamo il vecchio Chinino; è efficace contro tutte le specie di plasmodio, ha un costo relativamente basso, ma presenta difficoltà di somministrazione (endovena) che lo rendono poco utilizzabile in strutture carenti.
Nella storia della medicina occidentale, il primo medicamento efficace, impiegato per il trattamento della malaria fu la corteccia della pianta di Chincona, scoperta in Perù nel 1600 e importata in Europa dai padri gesuiti. Nel 1800 in Francia, i chimici Pelletier e Caventou dalla corteccia ottennero in forma pura il principio attivo anti-malarico, un alcaloide che fu chiamato chinino.
Gli effetti collaterali più frequenti sono conosciuti sotto il nome di Chinconismo (nausea, cefalea, vertigini, disturbi visivi ed uditivi) In alcuni casi si può osservare una perdita permanente dell’udito Il chinino stimola le cellule ß del pancreas, inducendo una ipoglicemia, soprattutto l’uso per via parenterale deve quindi essere accompagnato da somministrazione di glucosio per via endovenosa, sotto stretto monitoraggio dei valori glicemici.
E’ controindicato in pazienti con disturbi della conduzione cardiaca e non dovrebbe essere usato in pazienti digitalizzati oppure sotto terapia con warfarin
Fino alla scoperta della clorochina, è stato il principale farmaco nel trattamento della malaria. Ora sta tornando ad avere uno spazio dove si è sviluppata una resistenza alla clorochina.
posologia per il trattamento della malaria: 20mg/kg endovena in soluzione glocosata in ospedale, quindi continuare con 10mg/kg di peso ogni 8h per 7-10giorni.
Problemi legati all’accesso ai farmaci
Nonostante esistano farmaci di comprovata efficacia, molti Paesi africani continuano ad usare nei loro protocolli nazionali per curare la malaria la clorochina o il Fansidar, spesso in inutile associazione, anche quando si sono già sviluppate ampie resistenze. Ad oggi solo una ventina di Paesi africani ed asiatici hanno modificato i propri protocolli nazionali o hanno annunciato l’intenzione di farlo prossimamente introducendo l’ACT.
Molto spesso, pur tenendo nella massima considerazione il suggerimento di esperti mondiali di passare dalle vecchie ed inefficaci terapie a base di un solo farmaco a delle terapie con combinazioni di farmaci, sono costretti per mancanza di risorse ad accontentarsi di terapie meno costose.
La terapia ACT attualmente costa infatti molto di più di altre terapie standard: se il prezzo medio della vecchia terapia si aggira sui 0,10 centesimi di $, il prezzo più basso di tre giorni di terapia con ACT è $ 1,5, quindici volte più caro!
Inoltre, le scorte del farmaco sono ancora limitate. Alla raccomandazione dell’OMS di usare la ACT, dell’aprile del 2001, non è seguita la garanzia dei fondi necessari per stimolare i produttori europei, indiani, africani, vietnamiti e cinesi ad aumentare gradualmente la produzione. L’Organizzazione Mondiale della Sanità, i donatori e i governi coinvolti devono lavorare insieme per stimolare la produzione di ACT e collaborare con nuovi produttori, aiutandoli a soddisfare gli standard di qualità dell’OMS.
In Vietnam, dove cresce la maggior parte delle piante di Artemisia e dove si estrae la materia prima, gli agricoltori sono disposti a dedicare ancora più spazio a questa pianta remunerativa, se hanno la garanzia che vi sarà richiesta del prodotto………..
Bibliografia.
1. The Economic Burden of Malaria; John Luke Gallup e Jeffrey D. Sachs, American Journal of Tropical Medicine & Hygiene, genn/feb 2001 (supp.)
2. http://www.dpd.cdc.gov/DPDx/Default.htm
4. Malattie infettive; Moroni M, Esposito R, de Lalla F, ISBN: 88.214.2598.3 ed Masson ed2003
5. Efficiency of KAT-quick P.f. test (KAT medical, SAR) among the populations of drug-resistant parasites, Rabinovich SA, Le DK,, Med Parazitol (Mosk). 2006 Apr-Jun;(2):10-2.
6. Comparison of three diagnostic techniques for malaria: a rapid diagnostic test (NOW((R)) Malaria), PCR and microscopy ; Gatti S, Gramegna M. Bisoffi Z et all, Laboratory of Parasitology, Virology Service, Fondazione IRCCS Policlinico San Matteo, Viale Taramelli 5, 27100 Pavia, Italy Ann Trop Med Parasitol. 2007 Apr;101(3):195-204
7. Comparison of the OptiMAL test with PCR for diagnosis of malaria in immigrants, Iqbal J, sher A, et al J Clin Microbiol. 1999 Nov;37(11):3644-6
9. http://www.rollbackmalaria.org/
10. Argomenti di Epidemiologia 1, la malaria in Piemonte. 2006. Lorenza Ferrara, Daniela Lombardi, Roberto Raso, Servizio di riferimento Regionale di Epidemiologia per la sorveglianza, la prevenzione e il controllo delle Malattie Infettive – SeREMI
11. Safety of the insect repellent N,N-diethyl-M-toluamide (DEET) in pregnancy. McGready R et al. Am J Trop Med Hyg 2001 Oct;65(4):285-9)
12. Tolerability of malaria chemoprophylaxis in non-immune travellers to sub-Saharan Africa: multicentre, randomised, double blind, four arm study. Schlagenhauf P, Tschopp A,Johnson R BMJ. 2003 Nov 8;327(7423):1078
13. Atovaquone-proguanil versus mefloquine for malaria prophylaxis in nonimmune travelers: results from a randomized, double-blind study. van Genderen PJ, Koene HR, Spong K, Overbosch D. JTravel Med. 2007 Mar-Apr;14(2):92-5.
14. Post-marketing surveillance: adverse events during long-term use of atovaquone/proguanil for travelers to malaria-endemic countries.Overbosch D.J Travel Med. 2003 May;10 Suppl 1:S16-20
15. The safety of atovaquone/proguanil in long-term malaria prophylaxis of nonimmune adults.Petersen E. J Travel Med. 2003 May;10 Suppl 1:S13-5
16. Atovaquone-proguanil versus chloroquine-proguanil for malaria prophylaxis in non-immune travellers: a randomised, double-blind study. Malarone International Study Team.Hogh B, Clarke PD, Camus D, Nothdurft HD, Overbosch D, Lancet. 2000 Dec 2;356(9245):1888-94.
17. The efficacy and tolerability of doxycycline and mefloquine in malaria prophylaxis of the ISAF troops in Afghanistan.Sonmez A, Harlak A, Kilic S, Polat Z, Hayat L, J Infect. 2005 Oct;51(3):253-8.
18. Mefloquine and doxycycline malaria prophylaxis in Australian soldiers in East Timor.
Med J Aust. 2005 Feb 21;182(4):168-71Kitchener SJ, Nasveld PE, Gregory RM, Edstein MD.
19. Mefloquine compared with doxycycline for the prophylaxis of malaria in Indonesian soldiers. A randomized, double-blind, placebo-controlled trial.Ohrt C, Richie TL, Widjaja H, Shanks GD, Fitriadi J,Ann Intern Med. 1997 Jun 15;126(12):963-72.
20. Mefloquine versus doxycycline for malaria prophylaxis in intermittent exposure of Israeli Air Force aircrew in Rwanda.Shamiss A, Atar E, Zohar L, Cain Y. Aviat Space Environ Med. 1996 Sep;67(9):872-3
21. The efficacy of chemoprophylaxis against malaria with chloroquine plus proguanil, mefloquine, and atovaquone plus proguanil in travelers from Denmark.Kofoed K, Petersen E.J Travel Med. 2003 May-Jun;10(3):150-4.
22. www.malarone.com http://us.gsk.com/products/assets/us_malarone.pdf
23. http://www.traveldoctor.co.uk/malaria.htm
24. http://www.who.int/ith/countries/en/index.html
25. http://www.who.int/topics/malaria/en/